【小学科学 初中化学】吃皮蛋为什么要放醋?只是为了好吃?当然不是!
一、皮蛋的历史
要想弄清楚这个问题,就要了解一下皮蛋的历史。
皮蛋又称松花蛋、变蛋等,是以鸭蛋为主原料,再用生石灰、黄丹粉、茶叶末、纯碱、草木灰和食盐等加上调和稀包裹加工而成,具特殊风味,能促进食欲。
相传明代泰昌年间,江苏吴江县一家小茶馆,店主会做生意,所以买卖兴隆。由于人手少,店主在应酬客人时,随手将泡过的茶叶倒在炉灰中,说来也巧,店主还养了几只鸭子,爱在炉灰堆中下蛋,主人拾蛋时,难免有遗漏。一次,店主人在清除炉灰茶叶渣时,发现了不少鸭蛋,他以为不能吃了。谁知剥开一看,里面黝黑光亮,上面还有白色的花纹,闻一闻,一种特殊香味扑鼻而来;尝一尝,鲜滑爽口。这就是最初的皮蛋。
二、提出猜想
在小学科学、初中化学的学习中,同学们已经具备了酸碱的概念――在水溶液中电离出的阳离子全部是氢离子的化合物叫做酸,在水溶液中电离出的阴离子全部是氢氧根离子的化合物叫做碱。酸可以和碱发生中和反应,生成水和盐。

结合皮蛋制作的工艺:生石灰――主要成分为氧化钙(CaO)、纯碱――学名碳酸钠(Na2CO3,分类属于盐)、草木灰――草本和木本植物燃烧后的残余物,称草木灰,草木灰质轻且呈碱性。
我们猜想,王先生吃皮蛋被灼伤食道很有可能是因为其碱性太大,灼伤了食道!
那么问题来了!
1、猜想皮蛋碱性很强,那么普通生鸡蛋的pH是多少呢?
2、皮蛋究竟是否呈碱性?
3、食醋的pH为多少,它们可以中和吗?
4、皮蛋的蛋白和蛋黄的pH一样吗?
要想知道答案,那就跟随雪子一起动手做吧!
三、实验准备
1、基本物品:生鸡蛋2只、皮蛋2只、食醋、蒸馏水、烧杯、量筒、搅拌棒、铁架台、水果刀等;


2、数字化实验仪器:装有logger pro 3软件的电脑、数据采集器Labquest-Mini、pH传感器。
四、实验步骤
1、测量生鸡蛋的pH
(1)取两只生鸡蛋,打碎后倒入烧杯里搅拌均匀;



(2)用量筒量取200ml蒸馏水,倒入烧杯中搅拌均匀;

(3)搭建以下装置,测量生鸡蛋液的pH,保存数据。

2、测量皮蛋的pH
(1)取2只松花蛋去壳,分别切碎蛋白、搅碎蛋黄,倒入烧杯混合在一起;


(2)倒入200ml蒸馏水,搅拌均匀;

(3)搭建装置,测量皮蛋混合液的pH,保存数据。

3、测量食醋的pH
(1)用烧杯量取100ml食醋;

(2)搭建装置测量其pH,保存数据。

4、测倒入醋之后的皮蛋混合液pH
(1)将100ml醋倒入皮蛋混合液中,测量其pH,保存数据。


5、测量皮蛋蛋白的pH
(1)重新取2只皮蛋,剥下蛋白,切碎后倒入烧杯;

(2)倒入100ml蒸馏水,搅拌均匀;

(3)搭建装置,测量其pH,保存数据。


6、测量皮蛋蛋黄的pH
(1)取两只皮蛋蛋黄,在烧杯中碾碎;

(2)倒入100ml蒸馏水,搅拌均匀;


(3)搭建装置,测量其pH,保存数据。

五、实验数据
1、生鸡蛋的pH
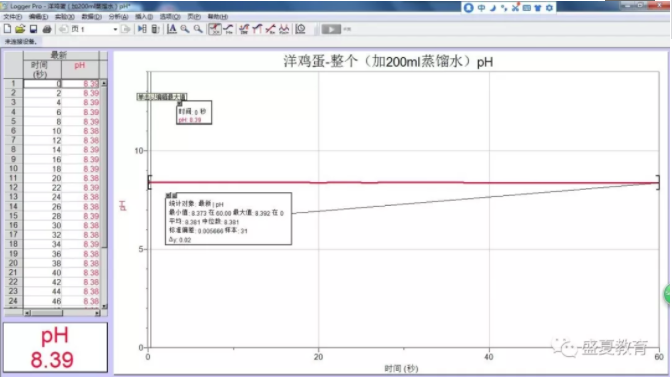
2、皮蛋的pH
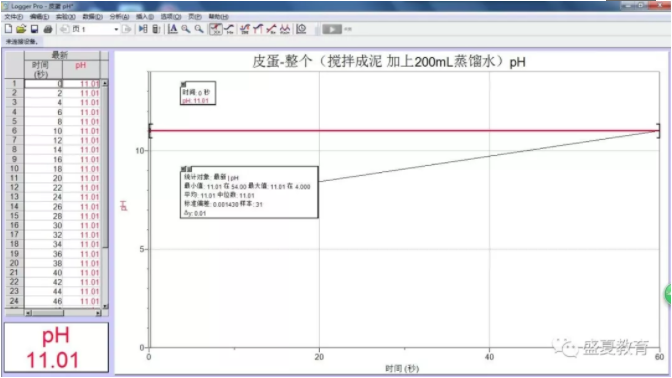
3、食醋的pH
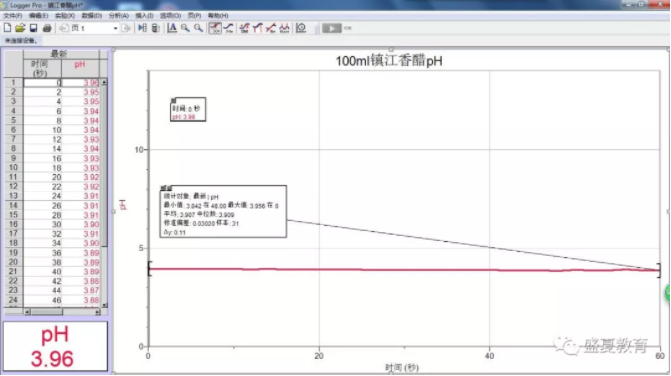
4、皮蛋混合液加入食醋后的pH
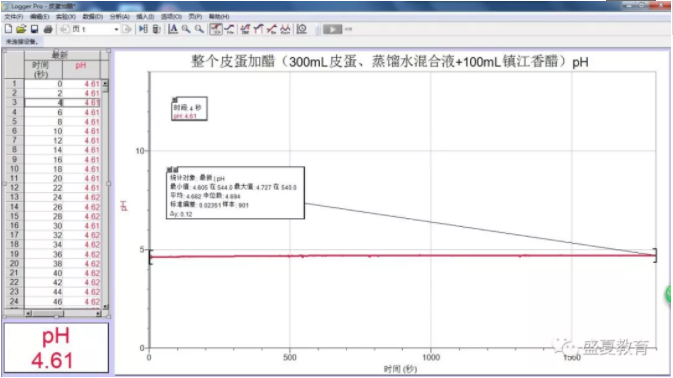
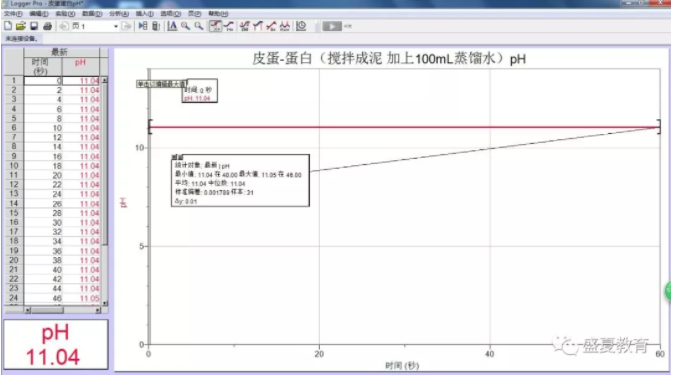
5、皮蛋蛋白的pH
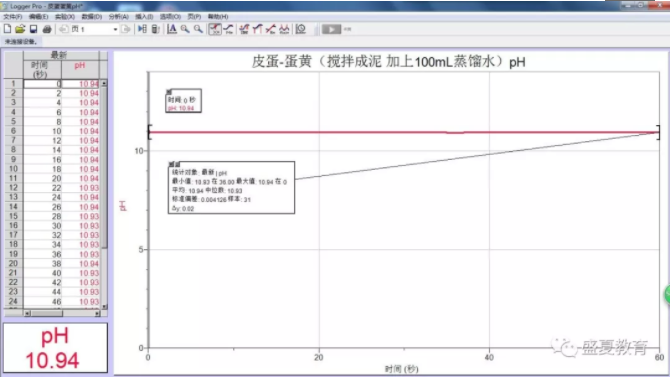
6、皮蛋蛋黄的pH
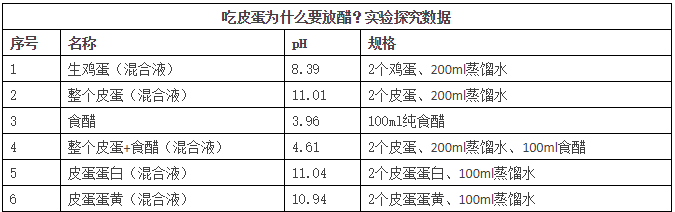
数据表格
|
|
|||
|
|
六、实验结论
1、生鸡蛋的pH为8.39,呈弱碱性;
2、对比生鸡蛋,皮蛋的pH为11.01,碱性很强,故由此证明我们的推断是对的,皮蛋碱性较强,直接食用的确可能灼伤肠胃;
3、食醋的pH为3.96,呈酸性;
4、当把食醋和皮蛋混合液混合后,pH变为4.61,介于皮蛋和食醋的pH数值之间。故可以判断,吃皮蛋放醋的确会产生酸碱中和,从而能够使得皮蛋的碱性变弱,不会损伤肠胃。但是食醋也不宜放太多,太多的酸对肠胃也不好;
5、皮蛋蛋白的pH略大于皮蛋蛋黄的pH,说明其碱性略强于皮蛋蛋黄。
七、拓展学习与思考
1、皮蛋特殊的风味是怎么来的?
答:蛋白质在氢氧根离子的作用下会逐渐分解成多种氨基酸,原本具有的含硫氨基酸被分解产生硫化氢(H2S,我们平时所说的臭鸡蛋气味的气体)及氨(NH3),再加上浸渍液中配料的气味,就产生特有的味道了。不过如果闻到皮蛋有很刺鼻的味道,很可能是氨含量太多,这个时候建议将皮蛋煮熟再食用,因为皮蛋制作时都会加入石灰和纯碱,在碱性溶液中,蛋白质会呈现凝胶特性,蛋白质在分解的过程中会产生氨。纯碱放得太多,氨就会多。
2、皮蛋上的松花是怎么来的?

答:蛋白的主要化学成分是一种蛋白质。禽蛋放置的时间一长,蛋白中的部分蛋白质会分解成氨基酸。他的化学结构有一个碱性的氨基-NH2和一个酸性的羧基-COOH,因此它既能跟酸性物质作用又能跟碱性物质作用。所以人们在制造松花蛋设计,特意在泥巴里加入了一些碱性的物质。如生石灰、碳酸钾、碳酸钠等。它们会穿过蛋壳上的细孔,与氨基酸化合,生成氨基酸盐。这些氨基酸盐不溶于蛋白,于是就以一定几何形状结晶出来,就形成了漂亮的松花。
3、皮蛋为什么会含铅?
答:加工松花蛋时,要将纯碱、石灰、盐、黄丹粉(黄丹粉含有氧化铅)按一定比例混合。
氧化铅在皮蛋加工中的作用有:
①促进和引导料液中的碱性成分渗入蛋内。
②使皮蛋转色快、色泽深、回味长。
③保持皮蛋蛋白的一定硬度,使皮蛋蛋白不粘壳、易脱壳。
④使皮蛋成熟期趋于一致,易于掌握,保证产品质量的稳定。
4、皮蛋蛋白的pH略高于皮蛋蛋黄的pH,这说明了什么?
答:根据数据判断,蛋白的碱性强于蛋黄的,说明在皮蛋的整个制作过程中,碱性浸渍液由外到内对皮蛋进行影响。但是二者差异并不大,所以为了保证碱性被全方位中和,吃皮蛋时我们通常习惯于把皮蛋切成一小瓣和醋凉拌,使其整体充分反应。
5、为什么剥完皮蛋,手上沾水后,会感到手上非常滑腻?
答:先前的实验我们已经证明了皮蛋里含有许多碱性成分,所以这和碱有关。
(1)碱性溶剂可以和使皮肤表面的油脂类化合物水解,生成脂肪酸盐;
(2)脂肪酸盐属于是表面活性剂,肥皂和洗衣粉都属于表面活性剂;
(3)表面活性剂是可以降低油水两相间的界面张力;
(4)皮肤表面角质层属于非极性(油性),而溶液中的溶剂是极性的(水);
(5)当我们单纯的用清水洗手由于界面张力会感到很涩,不那么滑腻;
(6)而我们用肥皂水或洗衣粉水洗手,由于油水间(皮肤与水之间)界面张力被降低,因此会感到滑腻感。