一定浓度醋酸溶液稀释时的pH变化
一定浓度醋酸溶液稀释时的pH变化
(指导老师 张强)
一、实验目的
1.掌握pH传感器的实时检测功能,并借助数据采集器和计算机直接生成数据曲线,便捷、直观地反映加水稀释过程中pH的变化。
2.认识醋酸加水稀释过程中pH突跃的变化,加深理解弱电解质电离的原理。
3.掌握pH变化曲线可用作研究弱电解质电离,并对其进行数学建模以及进行相关探讨。
二、实验背景
弱电解质加水稀释过程中pH的变化是学生在学习弱电解质电离时的一个难点,对于弱电解质越稀越电离的规律,学生理解起来非常抽象。利用pH传感器,实时检测溶液pH 的变化,能让学生很直观的看到整个加水稀释过程pH的变化,有助于学生理解加水稀释可以促进弱电解质电离的基本原理。
三、实验原理
向已知准确体积的一定浓度的醋酸溶液中加入水,将醋酸溶液体积稀释为原来的10倍,同时在整个过程中测定溶液的pH的变化,在快速加入水稀释的瞬间,醋酸溶液的pH会增加1,但很快pH会减少,这是由于加水稀释,醋酸继续电离出氢离子,导致溶液的pH又有所减少。
四、实验仪器和药品
实验药品:0.2 mol/L醋酸溶液、蒸馏水。
实验仪器:数据采集器、软件系统、pH传感器(已用标准缓冲液邻苯二甲酸氢钾溶液进行校准,pH=4.00)、磁力搅拌器、大烧杯。
五、实验步骤
1.用标准缓冲溶液校正pH传感器。
2.使用量筒量取50 mL 0.2 mol/L醋酸溶液于烧杯中。
3.向烧杯中放入小磁子,将烧杯放在磁力搅拌器上,开始搅拌。
4.用量筒量取450 mL蒸馏水。
5.再将洁净的pH传感器插入烧杯中的醋酸溶液中,并连接好数据采集器和电脑。
6.将量筒中的蒸馏水一次性快速倒入烧杯中,并同时测定溶液pH的变化。
7.完成稀释后,处置烧杯中的溶液。用蒸馏水冲洗pH传感器,清洗仪器。
8.利用软件处理得出醋酸稀释pH的变化曲线并加以分析。
六、结果讨论
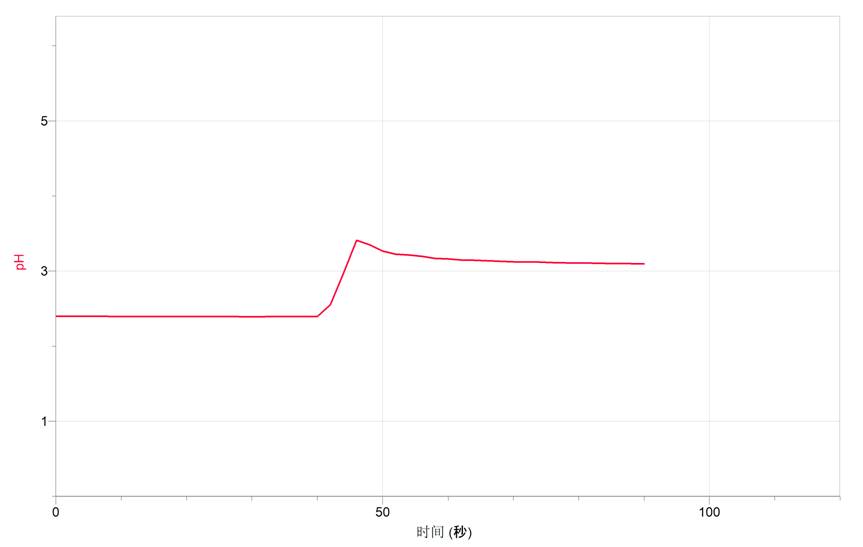
由图可准确看出在未加水之前,初始醋酸溶液的pH大约为2.4,加水稀释的瞬间溶液的pH增大到3.4,但接着溶液的pH又有所减少,最终pH大约为3.1。这是由于加水稀释的瞬间,醋酸溶液的浓度减少为原来的1/10,在这一瞬间氢离子的浓度也减少为原来的1/10,因此溶液的pH增大1,但由于加入了水,稀释了醋酸,会促进醋酸分子继续电离补充氢离子,因此溶液的pH又有所减少,但根据勒夏特列原理,平衡移动只能减弱原来的改变但不能完全抵消改变,所以pH不可能再减少和原来一样。通过曲线的测定可以给学生很直观的印象,帮助学生理解弱电解质的电离。